一款新药的获批上市,瞬间引爆了亚虹医药(688176)的股价。
3月3日晚间,亚虹医药披露公告称,公司收到国家药监局核准签发的药品注册证书,批准公司APL-1702(商标名:希维她®/CEVIRA®,通用名:盐酸氨酮戊酸己酯软膏宫颈光动力治疗系统)上市,用于治疗18岁及以上经组织学证实为子宫颈上皮内瘤变2级(CIN2)患者,排除子宫颈浸润癌和子宫颈原位腺癌。
公开信息显示,希维她®是一款全球首创、中国首发的光动力治疗产品,是全球首个针对宫颈上皮内瘤变2级(CIN2)患者的非手术无创治疗产品,填补了该治疗领域的临床空白。
公告介绍称,希维她®在治疗上具有精准靶向清除病变、HPV(人乳头瘤病毒)免疫清除、生育功能保护的独特优势,尤其是其无创治疗特质,可最大程度保全宫颈解剖结构和生理功能完整,使近60%患者延缓或避免手术,为适宜女性提供有效控制病变、保留生育功能的更优选择。
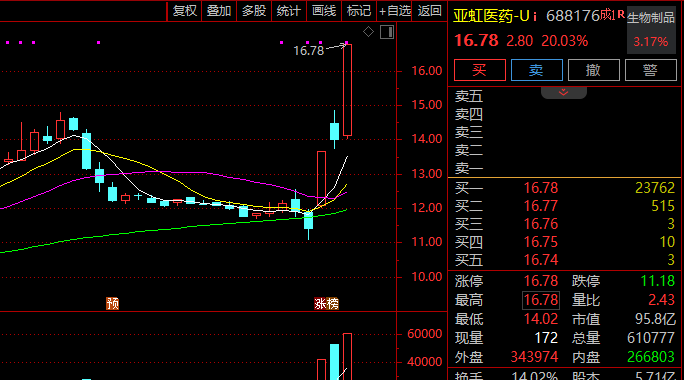
受此消息影响,亚虹医药于3月4日和3月6日双双“20cm”涨停,最近3个交易日累计涨幅超过47%。
3月6日晚间,亚虹医药发布股票交易异常波动公告称,经公司自查,公司目前生产经营活动正常,公司所处市场环境、行业政策没有发生重大调整,生产成本和销售等情况没有出现大幅波动,内部生产经营秩序正常。截至公告披露日,公司不存在涉及公司应披露而未披露的重大信息,不存在正在筹划重大资产重组、股份发行、债务重组、业务重组、资产剥离和资产注入等重大事项。

对于市场关注度较高的希维她®获批上市的情况,公告称,希维她®为境外生产药品,在公司取得该产品的上市批准后,方可开始逐步进行境外委托生产、进口、销售等环节。相关生产、进口的时间及程序均存在一定的不确定性,容易受到政策环境等多种因素的影响。
公司同时表示,该产品未来的销售主要产生于医院和双通道药房,前述市场的进入需要履行相关审核程序,且容易受到政策环境、市场需求及市场竞争等多种因素的影响,最终能否实现商业目标存在一定的不确定性。
亚虹医药还强调,医药产品具有高科技、高风险、高附加值的特点,药品的前期研发以及产品从研制、临床试验报批到投产的周期长,临床试验进度及结果、未来产品市场竞争形势均存在一定的不确定性。药品获得上市批准后的生产和商业化将受到政策环境、市场需求及市场竞争等多种因素的影响,存在一定的不确定性。请广大投资者谨慎决策,注意防范投资风险。